SimoažžÐg―ŌĘūïĘģŌōËØÅcADēĄĀíÉúÎïËÖūÎïĩÄČÔÚÂÏĩ
ëSÖøČŦĮōČËŋÚĀÏýgŧŊßMģĖĩÄžÓËŲĢŽ°Ē īÄšĢÄŽēĄĢĻAlzheimer's disease, ADĢĐĩÄžēēĄØúÕýģĘÖļĩžÔöéLĄĢĘĀ―įÐlÉú―Mŋĩþï@ĘūĢŽ2019ÄęČŦĮōADÏāęPÉįþģÉąūŌŅļßß_1.3Čf|ÃĀÔŠĄĢß@ŌŧĀūþŽF îīŲĘđŋÆW―įÆČĮÐĪÕŌÓÐЧĩÄžēēĄîA·ĀÅcļÉîAēßÂÔĄĢ―üÄęíĢŽÔ―íÔ―ķāĩÄŅÐūŋūÛ―đÓÚïĘģŌōËØÔÚAD°lÉú°lÕđÖÐĩÄŨũÓ×—ļßÖŽļßáÁŋïĘģ°éëSĩÄļßÉÅĘģŅŨ°YÖļĩĢĻDIIĢĐąŧŨCÅcADïLëUÕýÏāęPĢŽķøŌÔŋđŅŨéĖØÕũĩÄĩØÖКĢïĘģÄĢĘ―tÕđŽFģöï@ÖøĩÄÉņ―ąĢŨoЧŠĄĢŌÔÏÂÉíŅÐūŋÄēŧÍŽūSķČ―ŌĘūÁËïĘģÅcADēĄĀíÉúÎïËÖūÎïĩÄČÔÚÂÏĩĢŽé―ĻūŦĘïĘģļÉîAēßÂÔĖáđĐÁËÖØŌŠŋÆWŌĀþĄĢ

01 ĩØÖКĢïĘģĢšÄæÞDADēĄĀíĩÄČËČšŨCþ
Dietary patterns and blood-based biomarkers of Alzheimer’s disease in cognitively intact older adults: Findings from a population-based study
1ĄĒŅÐūŋąģū°ÅcÔOÓ
žČÍųŅÐūŋŌŅģõē―ŨCĩØÖКĢïĘģĢĻMediterranean Diet, MDSĢĐĩČŋđŅŨïĘģÅcÄX―ĄŋĩĩÄÏāęPÐÔĢŽĩŦïĘģÄĢĘ―ÅcADŅŠŌšÉúÎïËÖūÎïĩÄęPÂÐÔČÔČą·ĶīóŌÄĢČËČšĩþÖ§ģÖĄĢČðĩäøžŌĀÏýgŧŊÅcŨoĀíŅÐūŋĢĻSNAC-KĢĐĩÄß@íMāÃæŅÐūŋž{Čë1907Ãû≥60qĄĒo°VīôĮŌĩþÍęÕûĩÄÉį
^ĀÏÄęČËĢŽēÉÓÃηÖŨÓęÁОžÐgĢĻSimoaĢĐūŦĘzyŅŠĮåÖÐt-tauĄĒp-tau181ĄĒAβ42/40ĄĒNfLšÍGFAPĩČADšËÐÄÉúÎïËÖūÎïĢŽÏĩ―y·ÖÎöMDSŌĀÄÐÔž°ïĘģŅŨ°YÖļĩĢĻEDIIĢĐÅcÉÏĘöÖļËĩÄÏāęPÐÔĄĢ
2ĄĒÖũŌŠ―Yđû
MDSÅcADÉúÎïËÖūÎïĩÄęPÂĢšMDSŌĀÄÐÔÔ―ļßĢŽp-tau181šÍNfLËŪÆ――ĩĩÍĢĻĖáĘūtauĩ°°ŨēĄĀíØšÉpÝpŌÔž°Éņ―ÝSËũpûpÝpĢĐĢŧAβ42/40ąČÖĩtëSMDSŌĀÄÐÔĖáÉýķøÉýļßĢŽ·īÓģģöĩí·ÛÓĩ°°ŨģÁ·epÉŲĄĢīËÍâĢŽEDIIÖļĩÅcNfLËŪÆ―ģĘÕýÏāęPĢŽÕfÃũŅŨ°YïĘģÄÜžÓĄÉņ―pûĄĢ
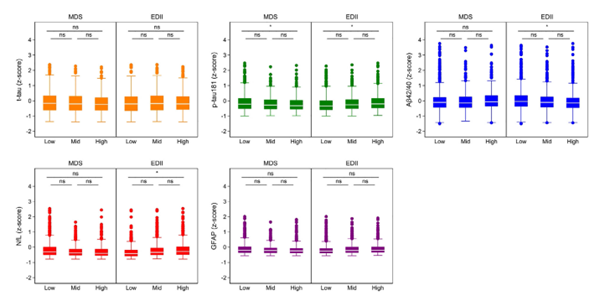 D1. ŧųÓÚĩØÖКĢïĘģÔu·ÖĢĻMDSĢĐšÍïĘģŅŨ°YÖļĩĢĻEDIĢĐČý·ÖÎŧĩĩÄŅŠŌšÉúÎïËÖūÎïËŪÆ―·Öēž
D1. ŧųÓÚĩØÖКĢïĘģÔu·ÖĢĻMDSĢĐšÍïĘģŅŨ°YÖļĩĢĻEDIĢĐČý·ÖÎŧĩĩÄŅŠŌšÉúÎïËÖūÎïËŪÆ―·Öēž3ĄĒŅÐūŋ―YÕÅcŌâÁx
ÔŅÐūŋĘŨīÎÔÚīóŌÄĢČËČšÖÐŨCĢšïĘģÄĢĘ―ÅcÕJÖŠÕýģĢĀÏÄęČËĩÄADēĄĀíÉúÎïËÖūÎïīæÔÚÃũī_ęPÂĢŽĮŌÔÚßzũŌŨļÐČËČšĢĻAPOE-ε4y§ÕßĢĐž°ļßýgČšówÖÐЧŠļüéÍŧģöĄĢß@Ōŧ°lŽFéĒĩØÖКĢïĘģŨũéADŌŧžîA·ĀēßÂÔĖáđĐÁËÁũÐÐēĄWŨCþĢŽÍŽrÕ{ÁËŧųÓÚßzũïLëUšÍÄęýg·ÖÓĩÄÐÔŧŊïĘģļÉîAĩÄÖØŌŠÐÔĄĢšóĀmÐčÍĻß^ŋvÏōŅÐūŋßMŌŧē―ōŨCÆäéLÆÚąĢŨoЧŠĄĢ
02 OmegaÖŽ·ūËáĢšŅÓūADßMÕđĩÄëpÜ·ĀÓųCÖÆ
Association of dietary fatty acids with longitudinal change in plasma-based biomarkers of Alzheimer’s disease
1ĄĒŅÐūŋąģū°
ąMđÜOmega-3ķāēŧïšÍÖŽ·ūËáĢĻPUFAsĢĐĩÄ°VīôîA·ĀŨũÓÃŌŅąŧģõē―ŨCĢŽĩŦÆäÅcADÉúÎïËÖūÎïŋvÏōŨŧŊĩÄęPÂÐÔČÔēŧÃũī_ĄĢČAĘĒîDļßĩØ-ŌōÎéĩÂļįąČĀÏýgŧŊíÄŋĢĻWHICAPĢĐĩÄĮ°Õ°ÐÔŅÐūŋĶ599Ãûŧųūo°VīôówßMÐÐÆ―ūų7.0ÄęĩÄëSÔLĢŽēÉÓÃSimoažžÐgÓBąOyŅŠ{p-tau181ĄĒAβ42/40ĄĒp-tau181/Aβ42ąČÖĩĄĒNfLž°GFAPĩČÖļËĢŽÏĩ―y·ÖÎöïĘģÖŽ·ūËázČëÅcADēĄĀíßMÕđĩÄrÐōęPÏĩĄĢ
2ĄĒÖũŌŠ―Yđû
Omega-3ÖŽ·ūËáĩÄÉņ―ąĢŨoЧŠĢšļßOmega-3zČë―MĩÄAβ42/40ąČÖĩÏÂ―ĩËŲÂĘï@ÖøpūĢĻĩí·ÛÓĩ°°ŨģÁ·eËŲķČ―ĩĩÍĢĐĢŧp-tau181ËŪÆ―ÔöéLËŲÂĘëSOmega-3zČëÁŋÔöžÓķøpÂýĢĻtauēĄĀíßMÕđ·ÅūĢĐĄĢ
Omega-6ÖŽ·ūËáĩÄ fÍŽąĢŨoŨũÓÃĢšOmega-6zČëÅcp-tau181ÔöéLģĘØÏāęPĢĻŌÖÖÆtauĩ°°ŨÁŨËáŧŊßMģĖĢĐĢŧļßOmega-6zČë―MGFAPËŪÆ―ÔöéLļüūÂýĢĻÉņ―ŅŨ°Y·īŠpÝpĢĐĄĢ
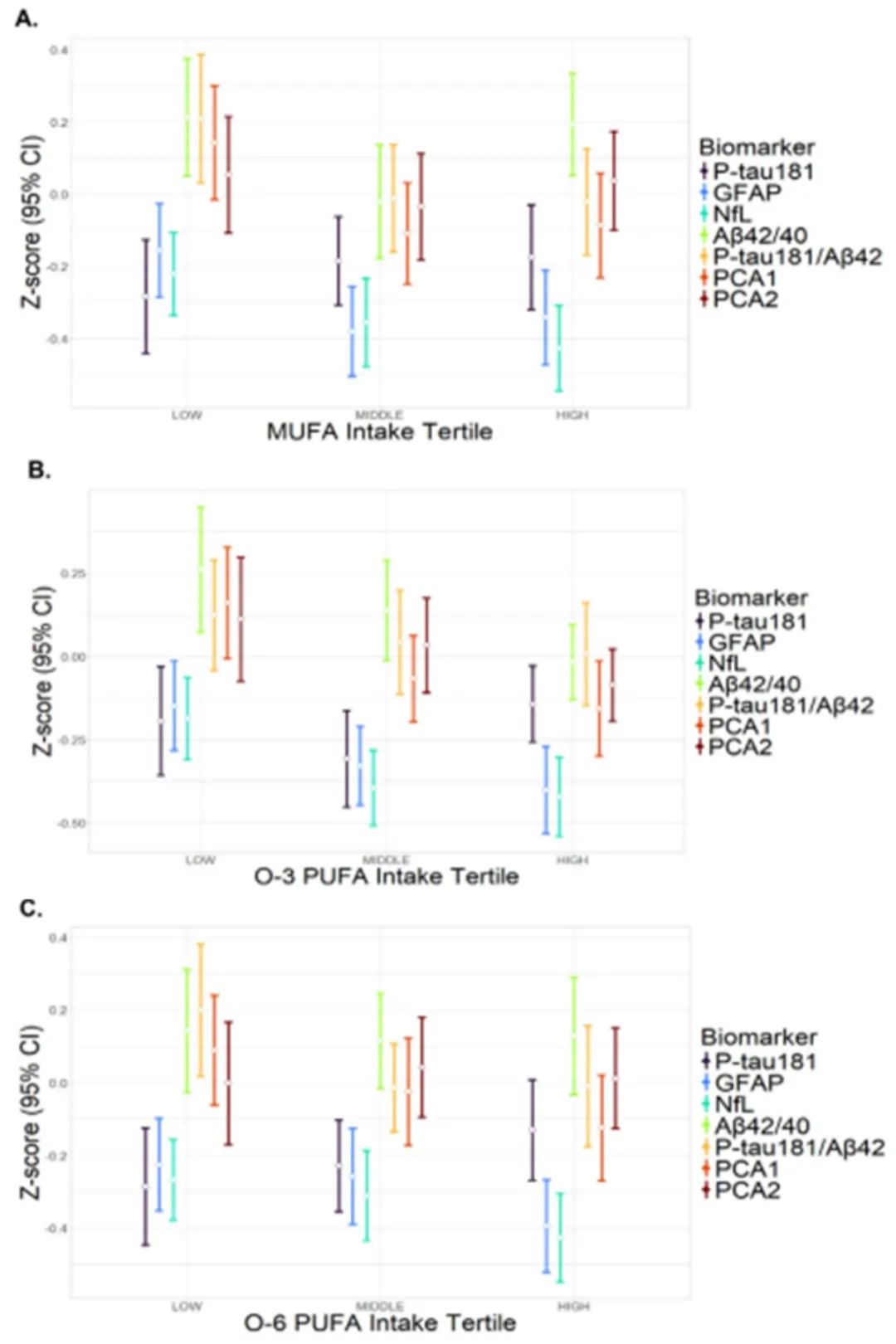 D2. °ī IðBËØzČëČý·ÖÎŧĩ·ÖĩÄŧųūÉúÎïËÖūÎïËŪÆ―
D2. °ī IðBËØzČëČý·ÖÎŧĩ·ÖĩÄŧųūÉúÎïËÖūÎïËŪÆ―3ĄĒŅÐūŋĒĘūÅcŠÓÃĮ°ū°
ÔŅÐūŋĘŨīÎÍĻß^éLÆÚëSÔLŨCĢšÝ^ļßĩÄŧųūOmega-3šÍOmega-6ÖŽ·ūËázČëÅcADŅŠŌšÉúÎïËÖūÎïĩÄūÂýßMÕđï@ÖøÏāęPĢŽĖáĘūļŧšŽīËî―ĄŋĩÖŽ·ūËáĩÄïĘģÄĢĘ―ĢĻČįô~îĄĒÖēÎïÓÍzČëĢĐŋÉÄÜģÉéŅÓūADēĄĀí·eĀÛĩÄÔÚļÉîAĘÖķÎĢŽÓČÆäÔÚžēēĄēĄĀíßMÕđÔįÆÚëAķÎЧđûļüéï@ÖøĄĢß@Ōŧ°lŽFé―ĻŌÔÖŽ·ūËáÆ―šâéšËÐÄĩÄïĘģîA·ĀēßÂÔĖáđĐÁËÖØŌŠŌĀþĄĢ
ŋ―YĢš
ÉíŅÐūŋÄēŧÍŽūSķČ―ŌĘūÁËïĘģŌōËØÅcADēĄĀíĩÄČÔÚÂÏĩĢšĩØÖКĢïĘģÄĢĘ―ÍĻß^ÕûówŋđŅŨЧŠÕ{đķā·NADÉúÎïËÖūÎïĢŽķøOmega-3/Omega-6ÖŽ·ūËátÍĻß^ĖØŪÐÔÕ{đĩí·ÛÓĩ°°ŨģÁ·eĄĒtauĩ°°ŨēĄĀíž°Éņ―ŅŨ°Yß^ģĖ°l]ąĢŨoŨũÓÃĄĢß@ÐĐ°lŽFđēÍŽÖ§ģÖ"ïĘģļÉîAŨũéADŌŧžîA·ĀēßÂÔ"ĩÄŋÉÐÐÐÔĢŽÍŽrÍđï@ÁËŧųÓÚówßzũąģū°ĢĻČįAPOEŧųŌōÐÍĢĐšÍÄęýgĖØÕũĩÄūŦĘ IðBļÉîAĩÄÖØŌŠÐÔĄĢ
ÎīíŅÐūŋÐčßMŌŧē―Ė―ËũĢšĒŲïĘģÄĢĘ―ÅcADÉúÎïËÖūÎïĩÄŌōđûęPÏĩĢŧĒÚēŧÍŽïĘģģÉ·ÖĩÄ fÍŽŨũÓÃCÖÆĢŧĒÛÄÉúÎïËÖūÎïļÄŨĩ―ÅRīēÕJÖŠđĶÄÜąĢŨoĩÄÞDŧŊ·―ĄĢß@ÐĐĖ―ËũĒéŨî―K―Ļ"ïĘģ-ŧųŌō-īúÖx"ČýÎŧŌŧówĩÄADîA·ĀówÏĩĩėķĻŋÆWŧųĩAĢŽÓÐÍûÔÚ―ĩĩÍžēēĄÉįþØú·―Ãæ°l]ęPæIŨũÓÃĄĢ
- ÖØ―MÏŲÏāęPēĄķū°ēČŦáĢŋ
- SimoažžÐg―ŌĘūïĘģŌōËØÅcADēĄĀíÉúÎïËÖūÎïĩÄČÔÚÂÏĩ
- ŋÕég―MWžžÐgÖúÁĶļßūŦķČ―âÎö·ÎĀwūSŧŊŋÕégŅÝŧŊ·―
- ImmPortĩþėÏÂÝd―ĖģĖĢšShared DataÄĢKĘđÓ÷―·Ļ
- AAV-RGDLRVSĶÖũÓÃ}ČÆĪž°ûĩÄÞDČūЧÂĘČįšÎĢŋ
- ķËÁĢÃļŧîÐÔzyĢšČūÁÏ·ĻÅc Taqman Ė―á·ĻĩÄąČÝ^ÅcÎīíÚ Ý
- AAVēĄķū°üŅbÁũģĖ―âÎö
- ÉúÎïÖÆËŪaÆ·ÖÐÄÄÐĐÓÆ·ÐčŌŠŨöÖ§ÔówzyÄØ
- ÉúÎïÐūÆŽŋÕégķā―MWÆ―Å_ÔŲĖíŌŧÅ_CosMx SMIģÉÏņÏĩ―y
- ÖÞĘŨÅ_CellXpress.aiÔÚÉÏšĢÉúÎïÐūÆŽÍęģÉŅbC
- SBC CosMX WTxΞ°ûŋÕégČŦÞDä―MÕýĘ―é_·ÅîAÓ
- ÉúÎïÐūÆŽÍÆģö"ÐūŋÕŌŧĖ"·―°ļÖØËÜŋÕégķā―MWзķĘ―
- IPHASEÕnĖÃé_ÕnĀēĢšžūúŧØÍÍŧŨÔōģĢŌî}Åc―âīð
- ÉúÎïÐūÆŽÅcÐūģŽÉúÎïšÏÍÆģö"ÐūŋÕŌŧĖ"ķā―MW·―°ļ
- ÉúÎïátËzyÅcÔĐđĐŠÉĖŌíšÍÉúÎïÏōČŦøÕÐÄž―äNÉĖ
- ūÉÏÕnģĖĢšØiÄcĩĀđÚ îēĄķūÅcČËówoÂĩÄīúÖxķ·