ŋÕég―MWžžÐgÖúÁĶļßūŦķČ―âÎö·ÎĀwūSŧŊŋÕégŅÝŧŊ·―

î}ÄŋĢšSpatial transcriptomics identifies molecular niche dysregulation associated with distal lung remodeling in pulmonary fibrosis.
ÆÚŋŊĢšNature genetics
IFĢš29
Doi: 10.1038/s41588-025-02080-x
ŅÐūŋąģū°
·ÎĀwūSŧŊĢĻPFĢĐĘĮŌŧîßMÕđÐÔ·ÎēŋžēēĄĢŽąíŽFéßhķË·Î―Mŋ―YšÍž°û―MģÉĩÄīóŌÄĢļÄŨĄĢĖØ°lÐÔ·ÎĀwūSŧŊĢĻIPFĢĐĘĮÆäÖÐŨîģĢŌĮŌŨîĀÖØĩÄîÐÍĢŽŧžÕßîAšóOēîĢŽķāĩÔÚÔ\āšó3ÖÁ5ÄęČËĀÍöŧōÐč·ÎŌÆÖēĢŽŽFÓÐĩÄÖÎŊĘÖķÎHÄÜēŋ·ÖpūēĄĮéĄĢ
IPFĩÄēĄĀíĖØücūßÓÐï@ÖøĩÄŋÕégŪŲ|ÐÔĢŽĀwūSŧŊĀÖØĩÄēĄÔîģĢÅc―YÏāĶÍęÕûĩÄ·ÎÅÝ―YÏāāīæÔÚĢŽąíŽFéēĄŨ·ĮÍŽē―°lÕđĄĢīËÍâĢŽIPF·ÎÖÐģĢģöŽFŪģĢĩÄ―üķËÉÏÆĪŧŊÉúĄĒðĪŌšÄŌÐÔ―Yž°ĀwūSÄļž°ûÔîĢŽß@ÐĐŽFÏóđēÍŽÍÆÓžēēĄßMÕđĄĢ
IPFēĄŨÔÚŋÕégÉÏīæÔÚķālēĒÐÐĩÄēĄĀíßMģĖĢŽÄŋÕégÉÏĀí―âž°û·Öēžž°·ÖŨÓégÏāŧĨŨũÓÃOéęPæIĄĢũ―yĩÄķā―MWžžÐgëyŌÔ―ŌĘū·Î―MŋĩÄž°ûÍësÐÔšÍŋÕégŪŲ|ÐÔĢŽąūŅÐūŋēÉÓÃļßž°û·ÖąæÂĘĩÄŋÕégÞDä―MžžÐgĢŽÏĩ―yĩØ―âÎöÁË·ÎĀwūSŧŊēĄÔîĩÄŋÕég―MŋžÜšÍ·ÖŨÓŅÝŨÜÛEĢŽ―ŌĘūÁË·ÎĀwūSŧŊß^ģĖÖÐķāëAķÎĄĒķā·―ĩÄēĒÐÐŅÝŧŊß^ģĖĄĢ
ÖũŌŠ―YÕ
1.ŋÕégÔÎŧyÐōĀLÖÆ·Î―MŋDŨVž°ĀwūSŧŊĖØÕũ
ĀûÓÃŋÕégÔÎŧzyžžÐgĢŽŅÐūŋFę Ķ45ßhķË·Î―MŋÓąūßMÐÐÁËž°ûžĩÄŋÕégąíß_·ÖÎöĢŽĀLÖÆÁËļēÉw47·Nž°ûîÐÍĄĒģŽß^160Čfž°ûĩÄ·Î―MŋDŨVĄĢŨReģö·ÎĀwūSŧŊß^ģĖÖÐķā·NęPæIĩÄž°û îBž°ÆäŋÕég·ÖēžĖØÕũĢš°üĀĻÎŧÓÚĀwūSŧŊ
^Óōß
ūĩÄ KRT5⁻/KRT17⁺ ÞDŧŊÐÍÉÏÆĪž°ûĢŽÅcā―üĩÄ CTHRC1⁺/FAP⁺ žĪŧîÐÍģÉĀwūSž°ûĢŽËüÔÚžēēĄÔįÆÚÐÎģÉÁË―Mŋ―YÖØËÜĩÄęPæI
^ÓōĄĢÍŽrĢŽÍíÆÚēĄÔîÖаlŽFĩÄ SPP1⁺ ūÞĘÉž°ûÔÚŋÕégÉÏÖðuČĄīúÁËÔÓÐĩÄ FABP4⁺ ČšĢŽ·īÓģÁËÃâŌßž°û―MģÉĩÄÓBÕ{ÕûšÍÖØËÜß^ģĖĄĢ
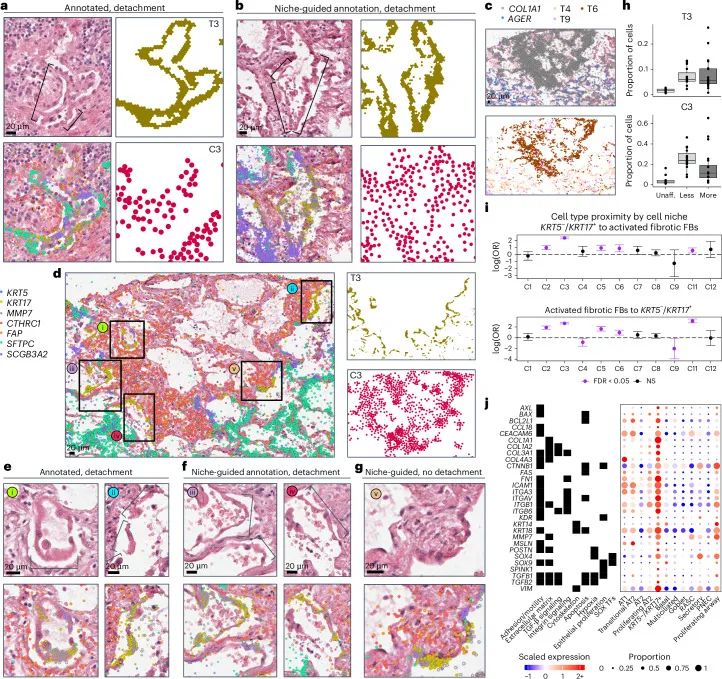 ·ÎĀwūSŧŊÖÐKRT5⁻/KRT17⁺ÞDŧŊÐÍÉÏÆĪž°ûÔÚĀwūSŧŊ
^Óōß
ūĩÄŋÕégķĻÎŧÅcÃëxĖØÕũ
·ÎĀwūSŧŊÖÐKRT5⁻/KRT17⁺ÞDŧŊÐÍÉÏÆĪž°ûÔÚĀwūSŧŊ
^Óōß
ūĩÄŋÕégķĻÎŧÅcÃëxĖØÕũ2.Visium HDōŨCģÉĀwūSž°ûÅcÆäËûž°ûÖŪégĩÄŋÕég·ÖēžĖØÕũ
éßMŌŧē―ōŨCËų°lŽFĩÄŋÕégąíß_ÄĢĘ―ĢŽŅÐūŋFę ßxČĄÆäÖÐÉĀýÓąūĢŽĀûÓà Visium HDŋÕégÞDä―MÆ―Å_ßMÐÐŅaģäōŨCĄĢ―Yđûï@ĘūĢŽÔÚĀwūSŧŊĮ°ū ^ÓōĢŽVisium HD Ãũī_ÍŽFÁË KRT17⁺ ÉÏÆĪž°ûÅc CTHRC1⁺ ģÉĀwūSž°ûĩÄŋÕégđēķĻÎŧĢŽÓĄŨCÁËĮ°ÆÚËų―ŌĘūĩÄÔįÆÚ―MŋĩÄÖØËÜ ^ÓōĄĢīËÍâĢŽVisium HD ÍŽÓzyĩ― FABP4⁺ Åc SPP1⁺ ūÞĘÉž°ûÔÚēŧÍŽēĄÔî ^ÓōĩÄŋÕég·ÖēžēîŪĢŽï@Ęū FABP4⁺ Åc SPP1⁺ ūÞĘÉž°ûÔÚēŧÍŽēĄÔî ^ÓōģĘŽFģöÃũï@ĩÄŋÕég·ÖēžēîŪĢŽ·īÓģÃâŌßž°ûČšów―MģÉšÍđĶÄÜ îBëSÖøžēēĄßMÕđ°lÉúëAķÎÐÔŨŧŊĄĢ
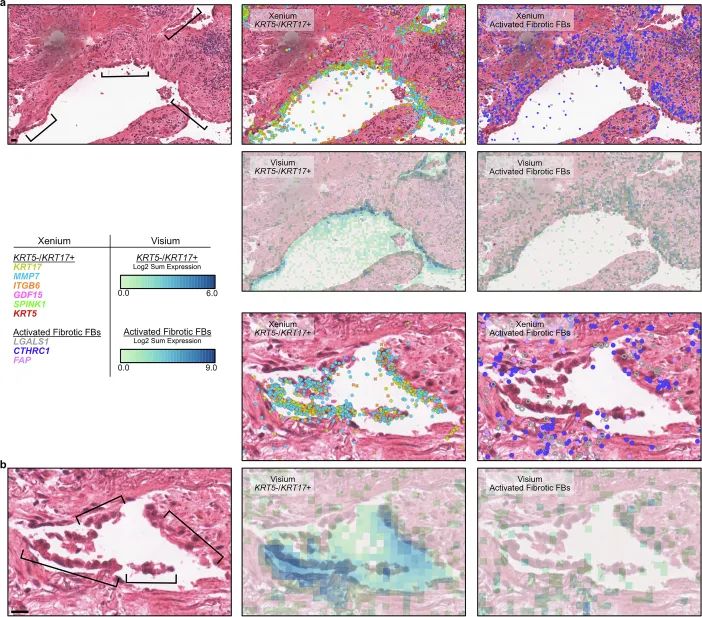 Visium HDōŨCĩÄ·ÎĀwūSŧŊÉúBÎŧÖÐKRT5⁻/KRT17⁺ž°ûŋÕégÃëx
Visium HDōŨCĩÄ·ÎĀwūSŧŊÉúBÎŧÖÐKRT5⁻/KRT17⁺ž°ûŋÕégÃëx3.CÆũWÁ―Ļ·ÎĀwūSŧŊĩÄŋÕégžžēēĄßMģĖÄĢÐÍ
ÔÚīËŧųĩAÉÏĢŽŅÐūŋFę ßMŌŧē―ŌýČëCÆũWÁËã·ĻĢŽĶ·ÎÅÝ―YßMÐÐŨÔÓŨReÅcŋÕégÖØ―ĻĢŽēĒ―YšÏž°û îBÅcŋÕég·ÖēžĩÄÓžęPÏĩĢŽ―ĻģöŌŧlÄ―Ąŋĩ·ÎÅÝ → ÉÏÆĪÔöÖģ → ž°ûÞDŧŊ → ģÉĀwūSŧîŧŊ → ÍíÆÚÃâŌß―þĩÄŋÕég“Îrég”ŅÝŧŊÝSĢĻŧųÓÚŋÕég―YÅÅÐō+ž°û îBŅÝŨ―ĻĩÄŋÕégÜÛEĢĐĢŽĮåÎúĩØÃčĀLģö·ÎĀwūSŧŊķāëAķÎĄĒķā·―ēĒÐÐŅÝŧŊĩÄß^ģĖĄĢūCšÏ·ÖÎöķā·Nž°ûĩÄŋÕég·ÖēžÅcÞDä îBĢŽŅÐūŋÃũī_ÁËÉÏÆĪž°ûÞDŧŊĄĒģÉĀwūSž°ûUÔöž°ÃâŌßŨVÏĩÞDQÔÚŋÕégÓžÖÐĩÄrégÐōÁО°ÏāŧĨÂÏĩĢŽ―ĻÁË·ÎĀwūSŧŊĩÄŋÕégžžēēĄßMģĖÄĢÐÍĢŽžÓÉîÁËĶ·ÎĀwūSŧŊēĄĀíŪŲ|ÐÔÐÎģÉCÖÆĩÄĀí―âĄĢ
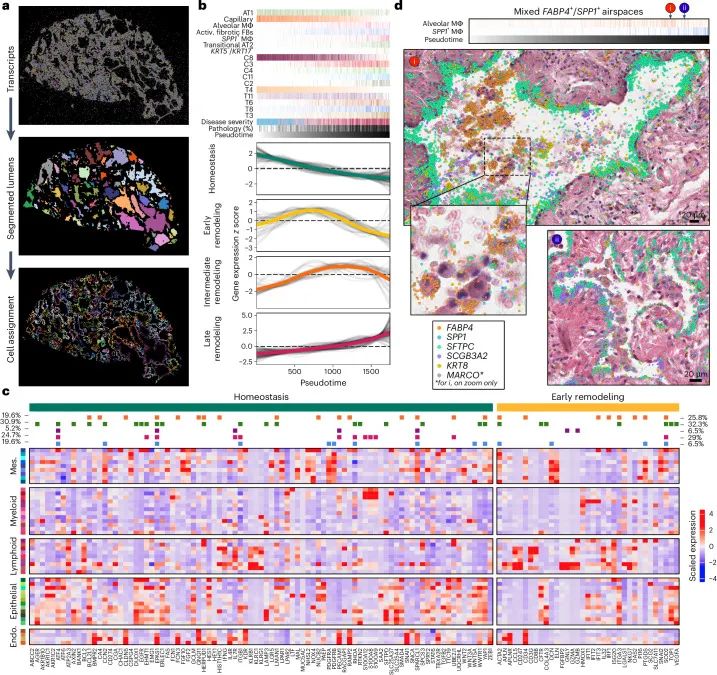 ŧųÓÚŋÕégÎÔŠ·ÖąæÂĘĩÄ·ÎÅÝÖØËÜ
ŧųÓÚŋÕégÎÔŠ·ÖąæÂĘĩÄ·ÎÅÝÖØËÜÎÄÕÂŋ―Y
ąūŅÐūŋĀûÓÃŋÕég―MWÆ―Å_ĢŽ―YšÏCÆũWÁËã·ĻĢŽŽFÁËĶĖØ°lÐÔ·ÎĀwūSŧŊÖÐķā·Nž°ûîÐÍĩÄūŦžÃčĀLĢŽÍŽr―ŌĘūÁËÆäž°ûžĩÄŋÕég·ÖēžĖØÕũĄĢÍĻß^Ïĩ―y·ÖÎö·ÎĀwūSŧŊß^ģĖÖÐęPæIž°ûČšĩÄŋÕégķĻÎŧž°ÓBŨŧŊĢŽ―ŌĘūÁË·ÎÅÝ―YÖØËÜĩÄķāëAķÎŋÕégßMÕđß^ģĖšÍķālēĒÐÐĩÄĀwūSŧŊßMÕđCÖÆĄĢŅÐūŋÍŧÆÆÁËũ―yūÐÔēĄģĖÄĢÐÍĩÄūÖÏÞĢŽĖáđĐÁË·ÎĀwūSŧŊÔÚķāŋÕégÎĒhūģÖÐēĒÐаlÕđĩÄÐÂŨCþĢŽŌēéūŦĘ·ÖÐ͚ͰÐÏōÖÎŊĖáđĐÁËÖØŌŠĩÄŋÕég·ÖŨÓŌĀþĄĢ
- ÖØ―MÏŲÏāęPēĄķū°ēČŦáĢŋ
- SimoažžÐg―ŌĘūïĘģŌōËØÅcADēĄĀíÉúÎïËÖūÎïĩÄČÔÚÂÏĩ
- ŋÕég―MWžžÐgÖúÁĶļßūŦķČ―âÎö·ÎĀwūSŧŊŋÕégŅÝŧŊ·―
- ImmPortĩþėÏÂÝd―ĖģĖĢšShared DataÄĢKĘđÓ÷―·Ļ
- AAV-RGDLRVSĶÖũÓÃ}ČÆĪž°ûĩÄÞDČūЧÂĘČįšÎĢŋ
- ķËÁĢÃļŧîÐÔzyĢšČūÁÏ·ĻÅc Taqman Ė―á·ĻĩÄąČÝ^ÅcÎīíÚ Ý
- AAVēĄķū°üŅbÁũģĖ―âÎö
- ÉúÎïÖÆËŪaÆ·ÖÐÄÄÐĐÓÆ·ÐčŌŠŨöÖ§ÔówzyÄØ
- ÉúÎïÐūÆŽŋÕégķā―MWÆ―Å_ÔŲĖíŌŧÅ_CosMx SMIģÉÏņÏĩ―y
- ÖÞĘŨÅ_CellXpress.aiÔÚÉÏšĢÉúÎïÐūÆŽÍęģÉŅbC
- SBC CosMX WTxΞ°ûŋÕégČŦÞDä―MÕýĘ―é_·ÅîAÓ
- ÉúÎïÐūÆŽÍÆģö"ÐūŋÕŌŧĖ"·―°ļÖØËÜŋÕégķā―MWзķĘ―
- IPHASEÕnĖÃé_ÕnĀēĢšžūúŧØÍÍŧŨÔōģĢŌî}Åc―âīð
- ÉúÎïÐūÆŽÅcÐūģŽÉúÎïšÏÍÆģö"ÐūŋÕŌŧĖ"ķā―MW·―°ļ
- ÉúÎïátËzyÅcÔĐđĐŠÉĖŌíšÍÉúÎïÏōČŦøÕÐÄž―äNÉĖ
- ūÉÏÕnģĖĢšØiÄcĩĀđÚ îēĄķūÅcČËówoÂĩÄīúÖxķ·