多通道電生理標測助力評估Man1a2敲低對抑郁模型中房顫發生的影響
研究背景:
抑郁癥是當代社會普遍且發病率上升的精神疾病,與心房顫動(AF)關聯密切,AF患者中抑郁癥患病率達38%-42.7%。流行病學研究均證實,抑郁癥是AF發病、新發生及復發的危險因素,也是導管消融術后AF復發的獨立危險因素。但兩者關聯機制尚不明確,目前僅知P2X7受體是連接因素。本研究基于無偏組學提出假設:抑郁狀態下腦白質分泌的N-棕櫚酰甘氨酸,通過Man1a2-AMPK-自噬-NRAP信號軸破壞心房閏盤,進而促進AF發生。
N-棕櫚酰甘氨酸由哺乳動物感覺神經元分泌,在組織器官中分布差異大,正常時皮膚和腦濃度最高,心臟含量極低,其生理功能尚未被充分探索。本研究發現,該物質可通過α1,2-甘露糖苷酶(Man1a2)作用于心肌閏盤,導致閏盤相關蛋白NRAP減少。Man1a2是參與真核蛋白N-糖鏈修飾的關鍵酶,其在內質網中的活性以劑量依賴方式決定錯誤折疊蛋白的降解途徑,局部濃度越高,蛋白錯誤折疊概率越大,而其在心肌組織中的作用此前未被報道。
基于此,哈爾濱醫科大學附屬第一醫院梁兆光教授團隊、董增祥教授團隊近期在Europace雜志上發表"N-palmitoyl glycine mediates depression-associated atrial fibrillation via Man1a2-dependent autophagy and NRAP dysregulation"文章。

研究結果:
1. 在CUMS誘導的抑郁大鼠中,AF的發生率增加
為驗證抑郁對房顫的影響,選用最常用、可靠且有效的慢性不可預知溫和應激(CUMS)嚙齒類抑郁模型。成功建立CUMS抑郁大鼠模型后,超聲心動圖評估顯示,抑郁大鼠左房舒張期內徑增大,E/E'升高。體表電生理檢測發現,抑郁大鼠心房有效不應期縮短,房顫誘導率升高。通過ELISA 檢測發現TNF-α表達升高。
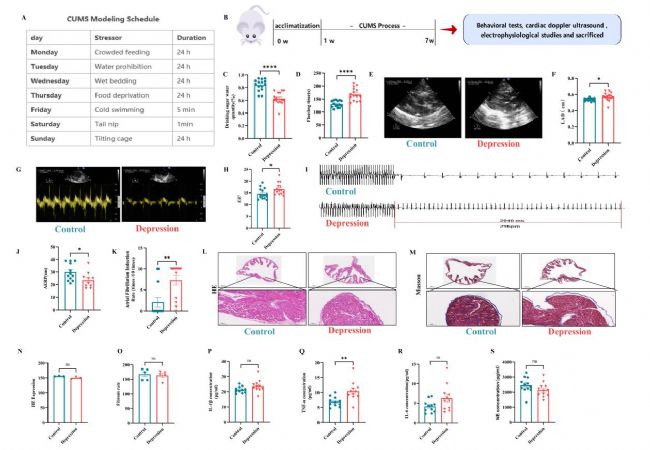
圖1 在CUMS抑郁模型大鼠中,左心房直徑和心房顫動(AF)誘導率均有所增加
2. 在CUMS誘導的抑郁大鼠及伴發AF的抑郁癥患者中,腦白質分泌的血漿及心房組織N-棕櫚酰甘氨酸水平均升高
為識別作用于心臟的神經系統代謝物,對抑郁大鼠和對照大鼠血漿進行全譜代謝組學分析,發現抑郁組代謝物中僅N-棕櫚酰甘氨酸由神經系統分泌。經LC-MS證實血漿中該物質由腦白質分泌。抑郁大鼠心房組織中該物質濃度也升高。臨床檢測顯示,伴房顫的抑郁癥患者血漿中N-棕櫚酰甘氨酸含量顯著高于單純抑郁癥患者。表明白質分泌的N-棕櫚酰甘氨酸在抑郁促發房顫中起重要作用。
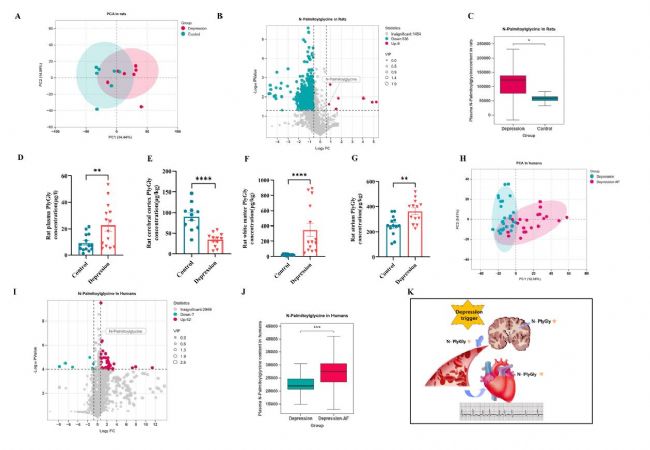
圖2 在抑郁腦白質中分泌的過量N-棕櫚酰甘氨酸作用于心房肌細胞
3. 在抑郁大鼠中,NRAP的減少可導致心房閏盤破裂
為探究抑郁狀態下心房組織中促進房顫發生的蛋白變化,進行蛋白質組學檢測。差異蛋白富集分析顯示,調控蛋白定位至細胞表面的蛋白顯著富集,心肌閏盤相關蛋白亦顯著富集。透射電鏡觀察發現抑郁大鼠心房肌閏盤破裂及肌漿網擴張。通過UniProt篩選出閏盤相關的NRAP表達下降最顯著。Western blotting及免疫熒光檢測均證實抑郁大鼠心房組織中NRAP表達顯著降低。
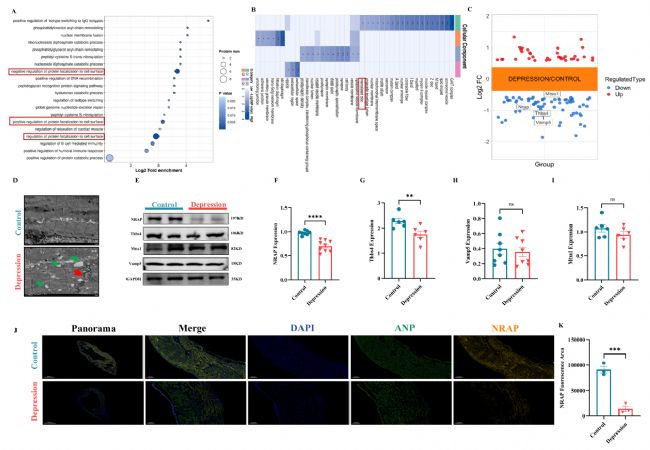
圖3 在CUMS模型中,NRAP的減少會導致心房閏盤破裂
4. 在抑郁大鼠的心房中,Man1a2的增加通過AMPK通路導致自噬水平降低
為探究NRAP減少機制,研究通過蛋白質組學分析發現,內質網與自噬相關降解途徑的差異蛋白中Man1a2表達增加。結合透射電鏡觀察,推測 Man1a2增加通過AMPK通路抑制自噬,致蛋白合成原料減少,進而阻礙NRAP合成。Western blot和免疫熒光檢測證實,抑郁大鼠心房組織中 Man1a2表達升高、AMPK激活且自噬水平降低。
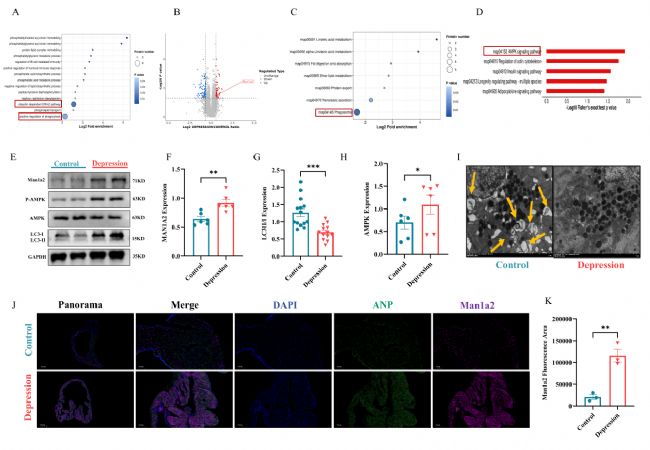
圖4 抑郁大鼠心房中Man1a2的增加通過AMPK通路導致自噬水平降低
5. 在體外實驗中,N-棕櫚酰甘氨酸通過AMPK通路抑制自噬,進而增加Man1a2并減少NRAP
在HL-1心房肌細胞中,N-棕櫚酰甘氨酸濃度超20μM具細胞毒性,其可濃度依賴性升高Man1a2表達。Man1a2在內質網蛋白糖基化中起關鍵作用,其增加雖提升蛋白折疊效率,卻也提高錯誤折疊概率,按生理需求此時需自噬途徑降解蛋白。但實驗顯示,N-棕櫚酰甘氨酸會使Man1a2增加,同時抑制AMPK介導的自噬,致自噬原料減少,NRAP表達下降,細胞免疫熒光亦證實此現象。這提示,該物質可能通過此路徑促進房顫。
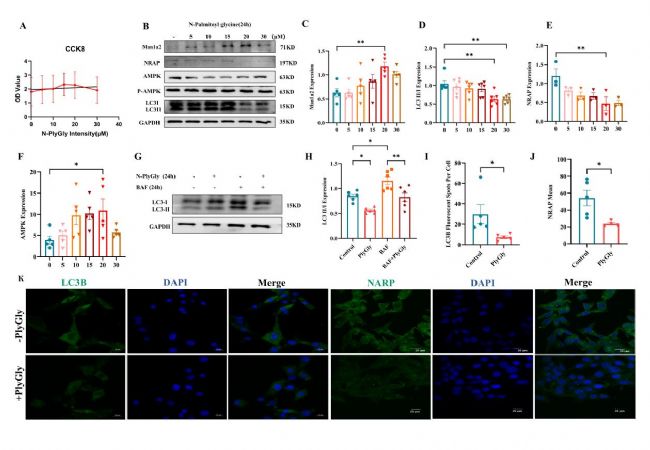
圖5 當將N-棕櫚酰甘氨酸添加到HL-1心房肌細胞中時,Man1a2表達增加,AMPK被激活,同時自噬水平和NRAP表達降低
6. 在體外和體內實驗中,敲低Man1a2可逆轉N-棕櫚酰甘氨酸所致的自噬水平降低及NRAP減少
研究通過體內外實驗證實,抑郁狀態下腦白質分泌的N-棕櫚酰甘氨酸進入血液,作用于心房組織,通過升高Man1a2表達激活AMPK信號通路,抑制自噬,導致閏盤相關蛋白NRAP表達下降,引起閏盤破裂,從而促進房顫發生。敲低Man1a2或激活自噬可逆轉這一過程,揭示了抑郁促發房顫的新機制。
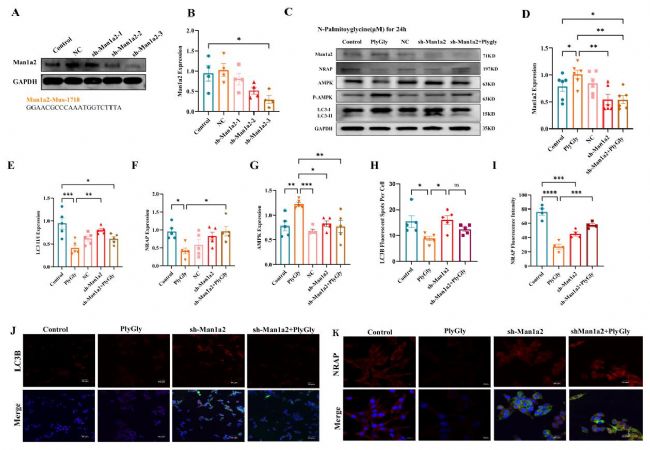
圖6 在體外實驗中,敲低Man1a2后,N-棕櫚酰甘氨酸所致的自噬水平降低和NRAP減少得以逆轉
7. Man1a2可作為靶點,用于降低抑郁誘導的AF的發生
為檢測該通路對心房電活動的影響及是否通過交感 / 副交感神經作用,采用多通道電生理標測技術,檢測Langendorff灌流后離體心臟的場電位信號。結果顯示,抑郁大鼠房顫誘導率和持續時間顯著增加,而Man1a2敲低組則降低。此外,CUMS抑郁大鼠左房電傳導離散度顯著增加,敲低Man1a2后異常傳導降低。這表明Man1a2可作為降低抑郁模型中房顫發生的靶點。
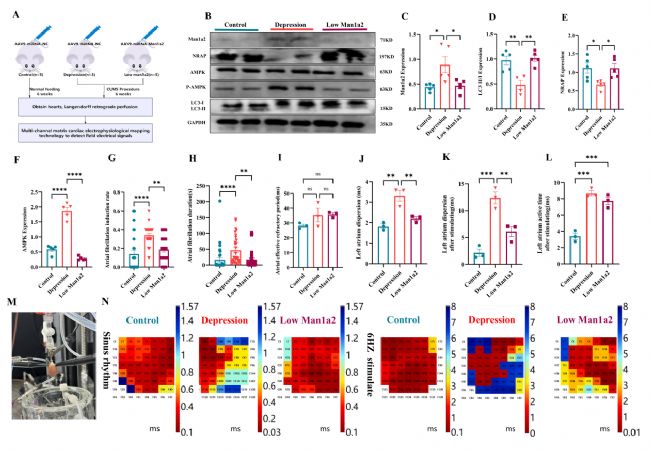
圖7 在抑郁大鼠中敲低Man1a2可逆轉自噬水平及NRAP
本研究證實,N-棕櫚酰甘氨酸通過升高Man1a2表達,減少心房肌細胞中AMPK相關自噬及NRAP表達,進而導致閏盤破裂和心房興奮傳導離散度增加,從而促進房顫發生。綜上所述,本研究闡明了腦白質分泌的N-棕櫚酰甘氨酸在抑郁誘發房顫發病機制中的作用,為防治抑郁相關房顫提供了新靶點。
本文通過多通道電生理標測技術對不同組大鼠離體心臟的房顫誘發率、持續時間、有效不應期以及傳導離散度等指標進行檢測,直接評估Man1a2敲低對抑郁模型中房顫發生的影響。