波形蛋白網絡失調:SNCA基因重復帕金森病神經原纖維缺陷的關鍵因素
《Science Advances》最新研究破解帕金森病神經突退化謎題:德國埃爾朗根大學團隊利用患者干細胞模型首次證實,SNCA基因重復通過劫持波形蛋白(vimentin)網絡導致神經突損傷,更發現兩種小分子藥物可逆轉病變。這一發現為帕金森病早期干預提供了全新靶點。

研究思路:
研究團隊從核心問題出發——SNCA基因重復如何損傷神經突? 通過三管齊下的策略破解謎題:首先利用CRISPR-Cas9技術在患者誘導多能干細胞(iPSC)中構建等基因對照組(SNCAIso) 消除遺傳背景干擾;接著通過多組學分析(轉錄組+蛋白組+表觀基因組)鎖定關鍵靶點;最終采用藥理學干預驗證治療潛力,形成完整證據鏈
研究方法和結果:
1. 基因編輯精準調控α-突觸核蛋白
揭示α-突觸核蛋白(aSyn)在神經前體細胞中的異常累積。團隊通過CRISPR技術成功將SNCA重復患者的基因表達恢復至正常水平,發現SNCADupl組神經前體細胞的aSyn蛋白升高,奠定致病基礎。
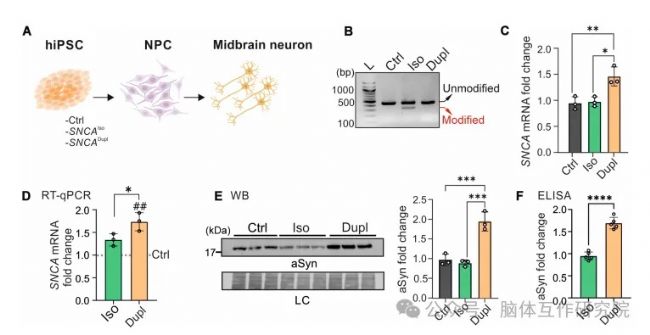
圖1 SNCADupl hiPSCs和NPCs中的aSyn水平
2. 時空失衡的α-突觸核蛋白動態
追蹤aSyn在神經元分化中的動態變化。時序監測顯示:分化早期aSyn異常升高,而分化后期雖總量下降,聚集態aSyn卻增加,且異常富集于神經突內,揭示時空失衡特征。
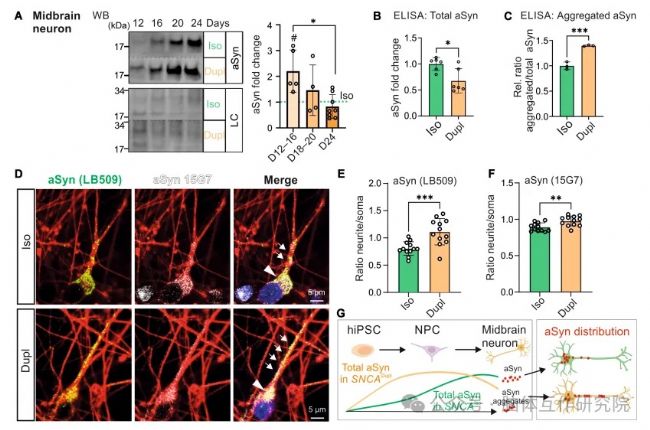
圖2 中腦神經元分化過程中的動態α-突觸核蛋白表達
3. 神經突三維結構坍塌
展現神經突結構的全面崩潰。三維成像發現SNCADupl組神經突密度下降、直徑縮減,關鍵骨架蛋白bTubIII表達降低。而基因校正后這些參數完全恢復正常,證明損傷的SNCA劑量依賴性。
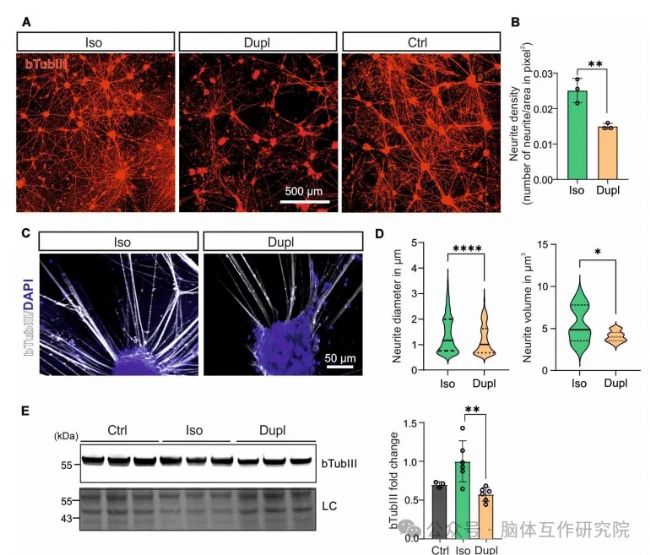
圖3 神經突與β微管蛋白III(bTubIII)水平的分析
4. 多組學鎖定元兇波形蛋白
通過多組學鎖定核心靶點。RNA-seq與蛋白質組學聯合分析顯示:VIM基因(編碼波形蛋白)表達上調,神經元分化調控因子PAX6顯著下調,且mRNA與蛋白變化高度相關,指明病理樞紐。
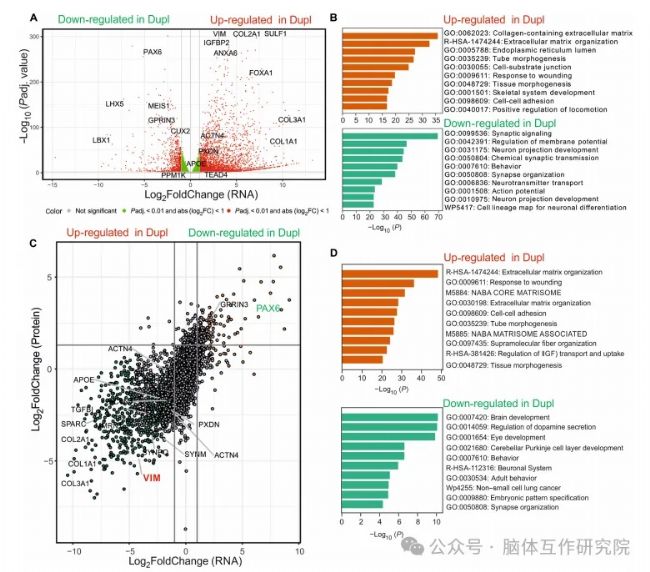
圖4 轉錄組學與蛋白質組學分析
5. 染色質開放度揭示調控漏洞
提供表觀遺傳調控證據。ATAC-seq分析發現VIM基因區染色質開放性增加,而PAX6啟動子可及性降低,闡釋基因表達紊亂的深層機制。
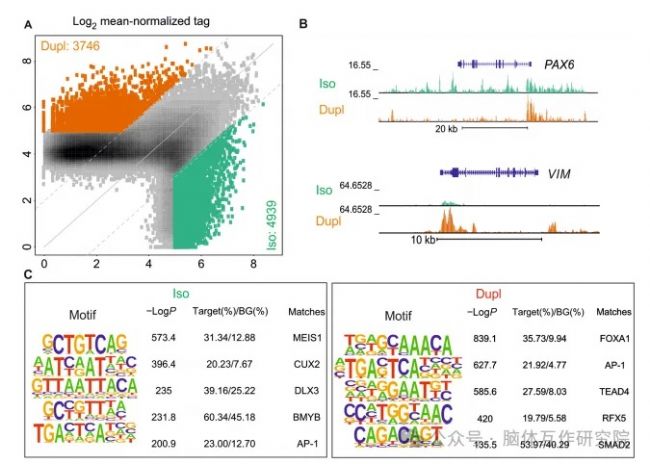
圖5 基于ATAC-seq技術的染色質可及性與轉錄因子結合位點富集分析
6. PAX6失活阻斷神經分化程序
證實分化程序持續受阻。質譜定量顯示SNCADupl組PAX6蛋白降低,該關鍵轉錄因子的失活導致神經分化程序全面失調。
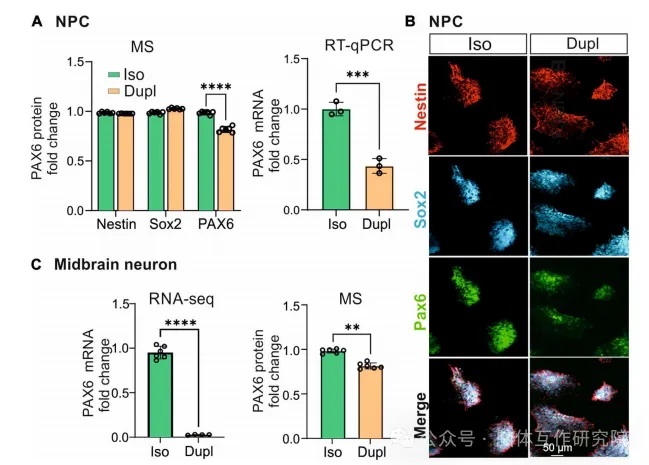
圖6 PAX6表達
7. 跨模型驗證波形蛋白崩解
揭示波形蛋白網絡的跨模型崩解。在患者干細胞、人腦組織及動物模型中均觀察到:波形蛋白出現異常截斷,神經突分布減少,且散發性帕金森患者腦組織重現相同病變,驗證臨床相關性。
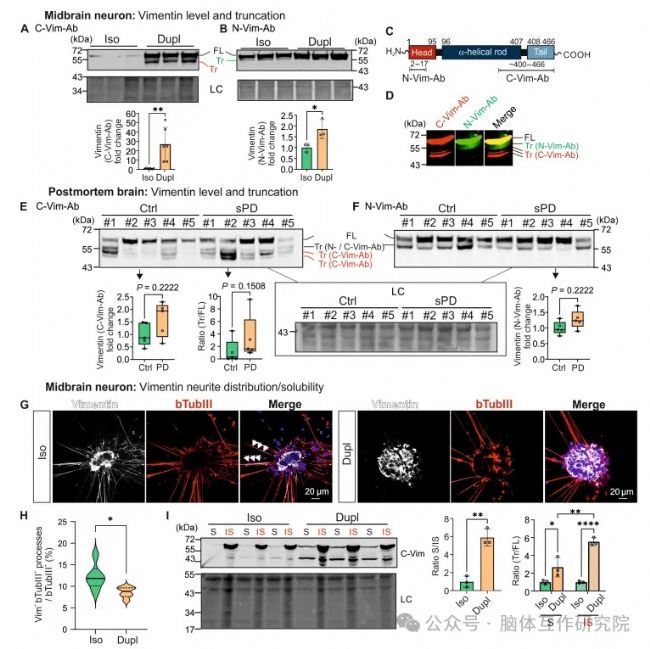
圖7 波形蛋白的表達、截短變異、亞細胞定位與組織結構
8. 小分子藥物成功修復神經突
實現小分子藥物逆轉損傷。使用岡田酸和睡茄素A干預波形蛋白后,截斷型蛋白減少,神經突直徑恢復至正常水平。突破性發現是:睡茄素A僅需2μM即可修復神經突體積,為治療提供實用方案。
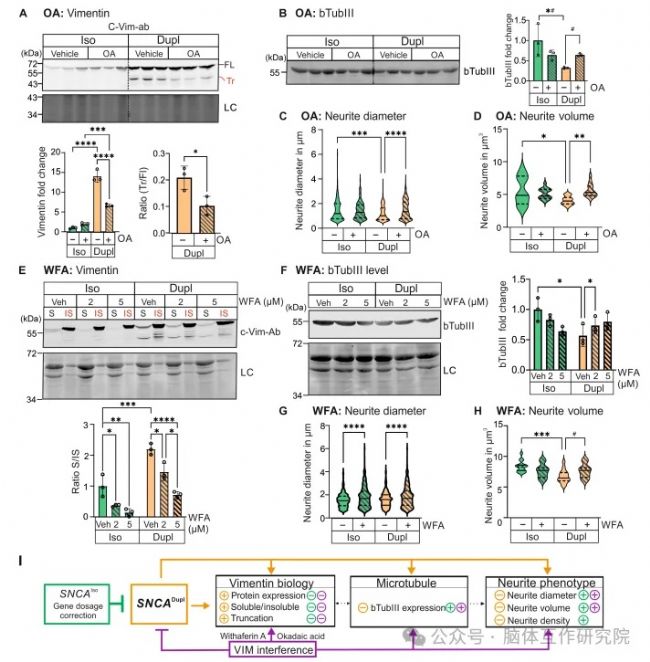
圖8 微管相關蛋白vimentin干擾對vimentin、βTubIII及神經突形態的影響
研究結論:
本研究首次繪制出SNCA重復→aSyn失衡→波形蛋白網絡解體→神經突損傷的完整致病軸心。更重要意義在于:靶向波形蛋白可繞過α-syn毒性直接修復神經突結構,為帕金森病早期干預開辟新路徑。相較于傳統聚焦神經元死亡的策略,該發現將治療窗口期大幅提前至神經突病變階段,具有重大臨床轉化價值。
參考文獻:
Schneider Y, Koller A, Schweigert A, et al. Vimentin network dysregulation mediates neurite deficits in SNCA duplication Parkinson's patient-derived midbrain neurons. Sci Adv. 2025;11(23):eadq2742. doi:10.1126/sciadv.adq2742 IF: 11.7 Q1
創作聲明:本文是在原英文文獻基礎上進行解讀,存在觀點偏向性,僅作分享,請參考原文深入學習。


想了解更多內容,獲取相關咨詢請聯系
電 話:+86-0731-84428665
伍經理:+86-180 7516 6076
徐經理:+86-138 1744 2250
郵 箱:consentcs@163.com