蛋白復合物CD3靶向藥雙抗的研發現狀及其在疾病診療中的意義
在人體免疫系統的精密運作中,CD3 作為關鍵角色,不僅是 T 細胞功能的核心參與者,更是當下癌癥免疫治療領域的熱門靶點。深入了解 CD3 的奧秘,對解鎖更高效的抗癌療法意義重大。
CD3 蛋白結構與信號轉導
CD3 是由 ε、γ、δ 和 ζ 四條多肽鏈組成的多聚體蛋白復合物,以 εγ、εδ、ζζ 三對二聚體的形式發揮作用,它緊密地與 T 細胞受體(TCR)非共價結合,是 T 細胞譜系的標志性特征。從結構上看,CD3 包含 N 末端胞外區、跨膜結構域以及含有免疫受體酪氨酸激活基序(ITAM)的胞質尾區。其中,CD3 ε、γ 和 δ 的細胞外結構域含有 lg 樣結構域,屬于免疫球蛋白超家族。
CD3 在 T 細胞活化過程中起著不可替代的作用。TCR - CD3 復合物在 T 細胞表面表達,TCR - αβ 特異性識別與 MHC 分子結合的同源肽抗原后,CD3 亞基將信號傳遞到細胞質內,激活一系列信號傳導事件。像 Lck 能使 ITAM 磷酸化啟動信號轉導,ZAP - 70 與磷酸化的 CD3 相互作用激活下游級聯反應,Nck、WASP 等也參與其中,共同調節 T 細胞的活化、分化。不過,TCR - CD3 復合物如何根據不同刺激產生多樣結果,目前仍是科研人員探索的方向,推測與招募的不同相互作用蛋白有關。

CD3 在疾病診療中的意義
在疾病領域,CD3 是惡性淋巴瘤、白血病(T 細胞腫瘤)分類的重要標志物,在乳糜瀉、淋巴細胞性結腸炎和膠原性結腸炎等病癥中,也能用于鑒定 T 細胞。值得關注的是,I 型糖尿病的易感性與 CD3 ε 基因座相關,抗 CD3 抗體在改善 I 型糖尿病及其他自身免疫性疾病癥狀方面展現出潛力。而系統性紅斑狼瘡(SLE)則與 CD3 ζ 多肽鏈缺陷存在關聯。
CD3 靶向雙抗的研發現狀
如今,CD3 靶向藥中雙抗的研究最為火熱。CD3 雙抗能夠引導 CD3 + T 細胞精準殺傷癌細胞,在癌癥免疫治療中發揮關鍵作用。目前,已有多款 CD3 雙抗獲批用于血液瘤治療。例如,安進 / 百濟神州的 Blinatumomab 是首個獲批上市的 CD3 雙抗,也是 BiTE 技術的首款藥物,但由于缺乏長效化設計,給藥不便,銷售額增長較為緩慢。近一年來,艾伯維的 Epcoritamab、羅氏的 Glofitamab 和 Mosunetuzumab、強生的 Teclistamab 等相繼獲批,進一步豐富了血液瘤的治療手段。

除已上市藥物外,眾多藥企還在積極布局 CD3 雙抗的研發管線。與 CD3 結合的熱門靶點包括 CD20、BCMA、CD19、EGFR 等。輝瑞和強生針對多發性骨髓瘤的雙抗已提交上市申請,強生的 Talquetamab 作為唯一進入 3 期的 GPRC5D 靶向藥,展現出不錯的療效,治療 3 線以上的客觀緩解率(ORR)達 74.1%。
臨床研究也在探索 CD3 雙抗在實體瘤治療中的應用,主要聚焦于 CEA、EGFR、EpCAM、HER2 和 PSMA 等經典腫瘤相關抗原(TAA)靶點。然而,CD3 雙抗研發面臨諸多挑戰。安全性方面,細胞因子釋放綜合征(CRS)和神經系統毒性較為常見,需要合理調控雙抗與 CD3 抗原的親和力。在實體瘤治療中,存在靶向的非腫瘤毒性、T 細胞浸潤不足、腫瘤微環境免疫抑制等障礙。不過,科研人員也在積極尋找解決方案,如選擇腫瘤特異性表達的 TAA、進行腫瘤微環境預處理、靶向免疫抑制細胞等,為攻克這些難題不斷努力。
CD3 作為雙抗靶點,在癌癥治療領域前景廣闊但挑戰重重。隨著研究的深入和技術的進步,相信未來 CD3 靶向雙抗將為更多癌癥患者帶來新的希望,推動癌癥治療進入新的階段。
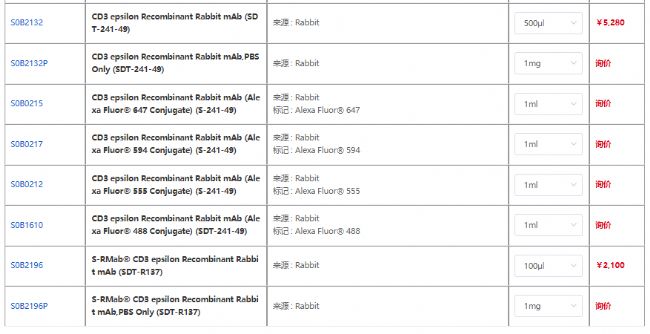
產品信息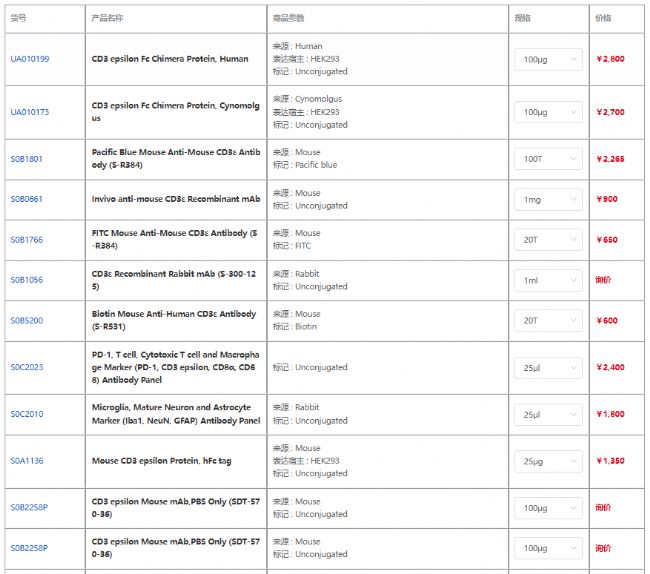
杭州斯達特 (www.starter-bio.com)志在為全球生命科學行業提供優質的抗體、蛋白、試劑盒等產品及研發服務。依托多個開發平臺:重組兔單抗、重組鼠單抗、快速鼠單抗、重組蛋白開發平臺(E.coli,CHO,HEK293,InsectCells),已正式通過歐盟98/79/EC認證、ISO9001認證、ISO13485。