時空組學技術在助力發現類風濕關節炎疾病治療新靶點中的應用

期刊:Arthritis and Rheumatology
影響因子:13.3
伯豪技術服務:時空組學
研究背景
類風濕關節炎(rheumatoid arthritis, RA)是一類自身免疫性疾病,其主要以多關節滑膜炎、血管翳形成以及軟骨與骨侵蝕為主要病理表現。生物制劑(bDMARDs)的應用讓大部分RA患者受益,但是仍然有30%-40%的患者對多種bDMARDs反應較差,揭示了RA中存在潛在的且未被重視的通路和靶點,以及對這些通路和靶點進行深入探索的必要性。與長期處于緩解期的RA患者相比,活動期的RA患者關節破壞的風險和進程明顯增加。因此,解析RA患者關節局部免疫微環境在活動期和緩解期的差異性,探索關節破壞的發生過程,對于保護RA患者的關節至關重要。
研究技術
ScRNA-SEQ,ST
研究內容
結合單細胞 RNA 測序 (scRNA-seq) 和空間轉錄組學,本研究對來自 3 名復發 RA 患者和 3 名緩解期患者的 6 個匹配的滑膜組織樣本進行了測序。使用 scRNA-seq 鑒定內襯和亞襯 FLS 子集;分析了復發期和緩解期之間 FLS 子集轉錄組的差異。差異分析表明,復發性 RA 患者的內膜 FLS 中成纖維細胞生長因子 (FGF) 通路高度激活,mIHC 證實 FGF10 表達增加。雖然 I 型干擾素通路也在內層 FLS 中被激活,但體外刺激實驗表明它獨立于 FGF10 通路。FLS 中 siRNA 敲低 FGF10 顯著降低 RANKL 的表達。此外,重組 FGF10 蛋白增強了原代人源血管翳細胞培養物中的骨侵蝕,而 FGFR1 抑制劑則減弱了這一過程。最后,施用 FGFR1 抑制劑在 CIA 大鼠模型中顯示出治療效果。
技術路線圖
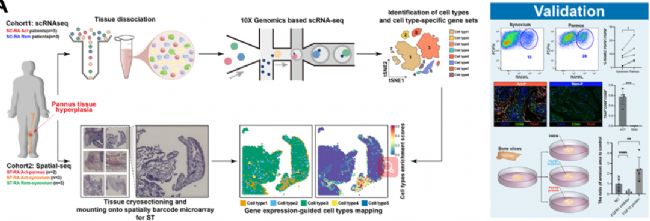
研究結果
1. 綜合 scRNA-seq 和 ST 分析揭示復發和持續緩解 RA 滑膜的時空景觀
為了研究復發和持續緩解 RA 的潛在病理機制,對來自三名復發 RA 患者和三名持續緩解 RA 患者的 6 個滑膜樣本進行了 scRNA-seq,并對 8 個配對樣本(復發 RA 中的 2 個血管翳樣本和 3 個滑膜樣本以及持續緩解 RA 中的 3 個滑膜樣本)進行了ST測序。經過數據預處理和嚴格的 scRNA-seq 數據質量控制后,獲得了來自復發 RA 患者 (n=3) 的 22,925 個細胞和來自持續緩解 RA 患者 (n=3) 的 32,236 個細胞用于進一步分析。首先進行了聚類分析,確定了 25 個簇,包括成纖維細胞(6 個簇)、內皮細胞(4 個簇)、骨髓細胞(5 個簇)、自然殺傷(NK)細胞(2 個簇)、肥大細胞(1 個簇)、B 細胞 (4個簇)、CD8+ T 細胞、CD4+ T 細胞和使用已建立的細胞標記基因的增殖細胞(圖 1B)。在滑膜細胞分數中觀察到復發組和緩解組之間的顯著差異。我們發現復發性 RA 中的 CD55+ 襯里成纖維細胞 (FB L-CD55)、T 細胞和 NK 細胞比緩解期的 RA 中高度富集(圖 1C )。同時分析了八個樣品的 ST 數據。我們使用無人監督的集群來分析血管翳和滑膜,并按細胞類型進行注釋(圖 1D)。我們發現位于血管翳內層的 CD55+ 內層成纖維細胞數量豐富(圖 1E)。
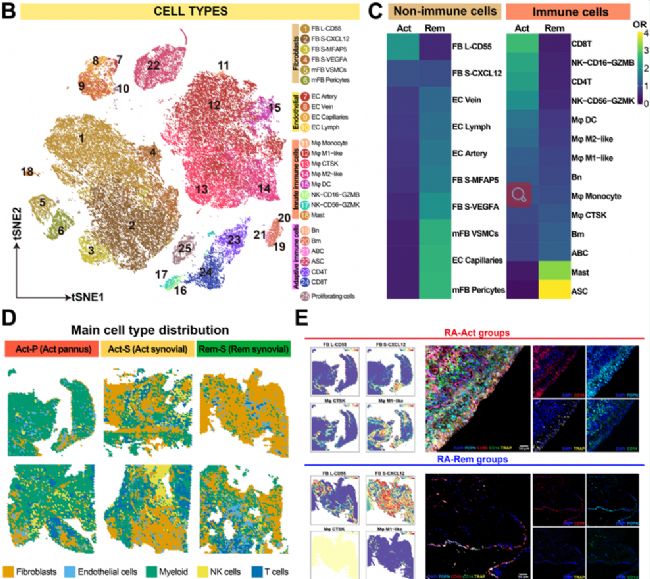
圖1
2. 復發和緩解 RA 的 FLS 子集顯示出不同的激活途徑
鑒于 FLS 在 RA 發病機制中的關鍵作用,研究特別關注 FLS 亞群在 RA 復發和緩解中的作用。經過質量控制,獲得了 22,679 個高質量的 FLS,根據差異表達基因 (DEG) 將其分為四個子集:CD55+ 襯里成纖維細胞 (FB L-CD55)、CXCL12+ 亞襯成纖維細胞 (FB S-CXCL12)(圖 2A 和 C) 、MFAP5+ 亞襯成纖維細胞 (FB S-MFAP5) 和 VEGFA+ 亞襯成纖維細胞 (FB S-VEGFA)(圖 2A)。通過整合單細胞測序數據和公共數據庫的數據,觀察到復發性 RA 中 CD55+ 內襯成纖維細胞的比例很高,這表明內膜成纖維細胞在復發 RA 中顯著增殖(圖 2B)。通過對DEG 進行聚類來生成熱圖,以深入了解復發和緩解 RA 中 FLS 的四個子集的分子特征差異(圖 2D)。發現 FB L-CD55 和 FB S-CXCL12 在復發和緩解 RA 之間存在顯著差異。FB L-CD55 表達與基質金屬蛋白酶 (MMP) 和脂多糖結合蛋白 (LBP) 相關的基因, MMP加速軟骨降解, LBP表明復發 RA 中先天免疫反應的上調(圖 2D)。FB S-CXCL12 在復發性 RA 中表達與 MHC II 類呈遞和補體激活途徑 (C3) 相關的基因(圖 2D)。接下來,研究基于 Hallmark 和 Reactome 數據集對 FLS 子集進行了通路分析(圖 2E)。發現,來自復發性 RA 的 FB L-CD55 中的干擾素 α (IFN-α)、干擾素 γ (IFN-γ) 和成纖維細胞生長因子受體 1 (FGFR1) 通路高度激活。在緩解期 RA 中,FB L-CD55 和 VEGFA+ 成纖維細胞 (FB S-VEGFA) 中高度富集凋亡和缺氧途徑。這些數據表明,FLS 亞群具有不同的基因表達模式,受不同的復發和緩解 RA 途徑調節。
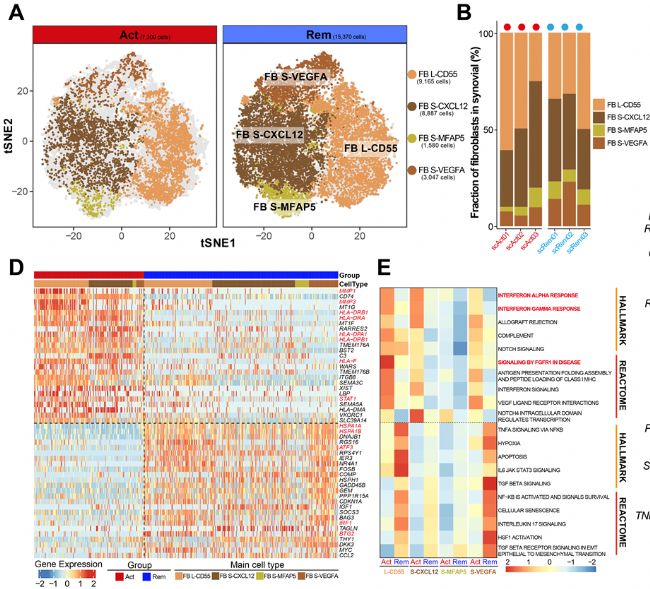
圖2
3. FGF10-FGFR1信號通路在復發性RA的內層FLS中異常激活
CellChat 分析顯示,FB L-CD55 與復發 RA 中的其他 FLS 子集具有強烈的 FGF 信號通路相互作用(圖 3A)。此外,研究觀察到 FGF10-FGFR1 對在復發 RA 的 FB L-CD55 中高度激活(圖 3B,左)。對于亞襯FLS,FGF7-FGFR1 對占主導地位;然而,復發和緩解 RA 之間沒有明顯差異(圖 3B,右)。對不同 FLS 亞群中 FGF7、FGF10 和 FGF14 轉錄組表達水平的進一步分析表明,FGF10 在復發 RA 的 FB L-CD55 細胞中高表達(圖 3C)。使用 mIHC,研究確認 PDPN+FGF10+ FLS 主要在復發 RA 的血管翳內層中檢測到(圖 3D)。通過 IHC 對復發和緩解 RA 患者的 12 個血管翳樣本中的 FGF10 表達進行定量分析顯示,復發 RA 患者中 FGF10 陽性區域的比例顯著高于緩解 RA 患者(圖 3E 和 F)。通過結合 scRNAseq 和 IHC 數據,證明了復發 RA 內膜 FLS 中 FGF10-FGFR1 信號通路的過度激活。
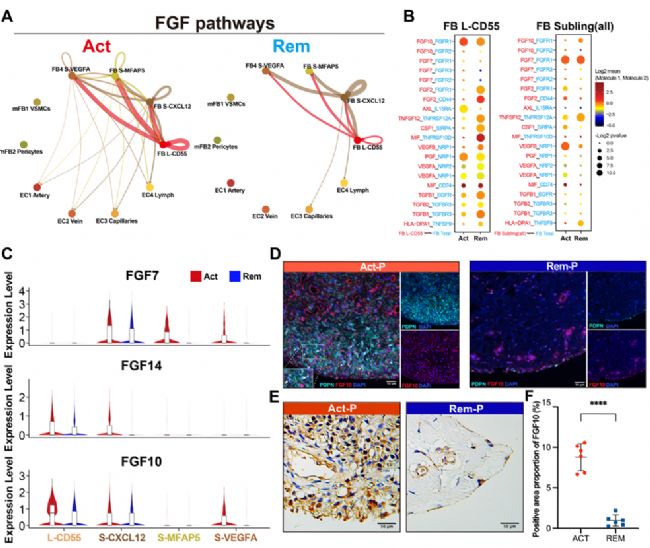
圖3
4. IFN-α和FGFR1信號通路在復發性RA中很大程度上是獨立的
鑒于 IFN-α 和 FGFR1 信號通路主要在復發 RA 的內層 FLS 中激活,本研究探討了這兩種通路之間是否存在交叉調節。首先,通過比較來自 scRNA-seq 數據的 FLS 中的兩個通路評分來進行相關性研究。未觀察到 IFN-α 和 FGFR1 信號通路與總 FLS 或復發或緩解 RA 的 FLS 之間存在任何已建立的相關性 (R>0.3)(圖 4A 和 B)。這些結果表明這兩條途徑在單細胞水平上很大程度上是獨立的。
為了證實這些發現,進行了體外刺激實驗。用重組人干擾素α2a(IFN-α2a)或FGF10蛋白刺激MH7A FLS細胞系6小時,并通過qRT-PCR測量目標分子。與未刺激的對照組相比,IFN-α2a刺激MH7A FLS細胞系以劑量依賴性方式誘導了預期的IFI6和ISG15 mRNA表達;然而,沒有觀察到 FGF10 mRNA 的顯著變化(圖 4C)。同時,用 10 ng/ml 和 100 ng/ml FGF10 刺激 MH7A FLS 細胞系對 IFI6 和 ISG15 mRNA 的表達幾乎沒有影響(圖 4D)。總的來說,本研究提供了初步證據表明 IFN-α 和 FGFR1 信號通路不太可能相互交叉調節。
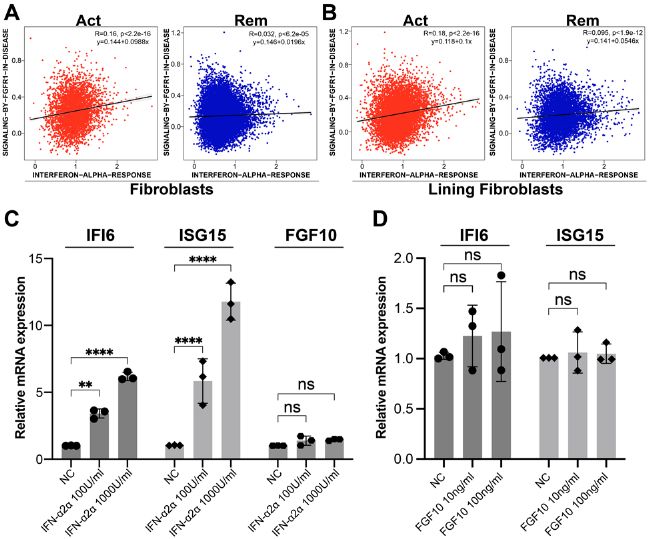
圖4
5. 襯里 FLS 中的 IFN-α 和 FGFR1 信號通路與復發 RA 中的不同代謝通路存在差異相關
既往對RA和OA滑膜成纖維細胞代謝的研究表明,缺氧和糖酵解是RA滑膜成纖維細胞的特征。研究觀察到復發和緩解 RA 中的 FLS 亞群表現出不同的代謝活動(圖 5A)。在襯里成纖維細胞(FB L-CD55)中高度富集的代謝途徑中,花生四烯酸代謝、亞油酸代謝、氧化磷酸化、泛酸和CoA生物合成在復發性RA中占主導地位。相比之下,煙酸鹽和煙酰胺代謝、半胱氨酸和蛋氨酸代謝以及糖酵解/糖異生在 RA 緩解中普遍存在。
相關分析顯示,IFN-α信號通路與亞油酸、α-亞麻酸和花生四烯酸代謝密切相關(圖5B和C)。相反,FGFR1信號通路與代謝通路的相關性較小,與賴氨酸降解和粘蛋白型O-聚糖生物合成的相關性較弱(圖5B和D)。這些數據表明 IFN-α 和 FGFR1 信號通路與復發性 RA 襯里 FLS 中的不同代謝通路相關。
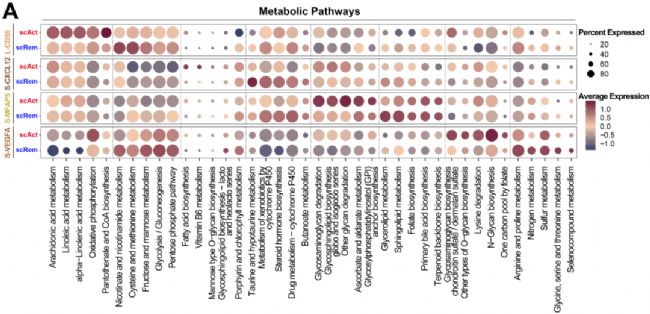
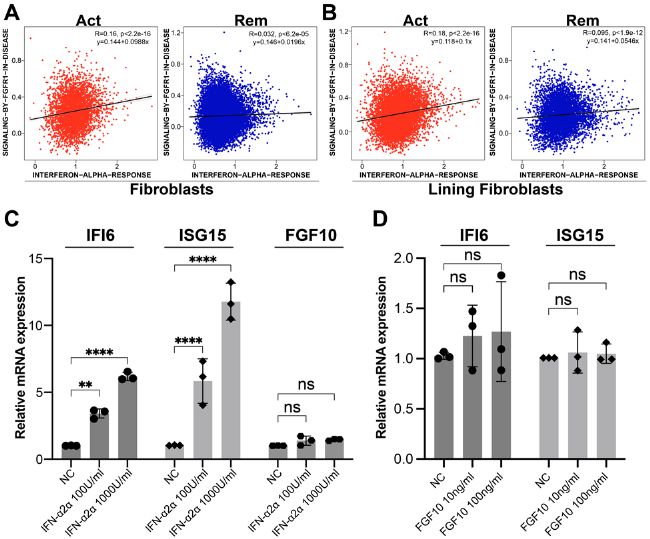
圖5
6. 阻斷 FGFR1 信號通路可減輕體外骨侵蝕,并在大鼠關節炎模型中顯示治療效果
研究進行 Transwell 侵襲實驗來探討 FGF10/FGFR1 信號在 FLS 侵襲性中的潛在作用。與siNC和siFGF7相比,siFGF10顯著抑制FLS的侵襲能力(圖6A和B)。通過蛋白質印跡進一步測量了與 FLS 侵襲性相關的幾種基質金屬蛋白酶 (MMP)。結果顯示,與siFGF7和siNC相比,siFGF10顯著抑制MMP2的表達(圖6C和D)。基于此,假設 FGF10/FGFR1 信號傳導促進復發性 RA 中 FLS 的侵襲性,并且 MMP2 參與了這一過程。除了MMP2之外,發現與siFGF7和siNC相比,siFGF10強烈抑制RANKL的表達(圖6C和D),這表明FGF10/FGFR1途徑可能參與復發性RA的破骨細胞生成。
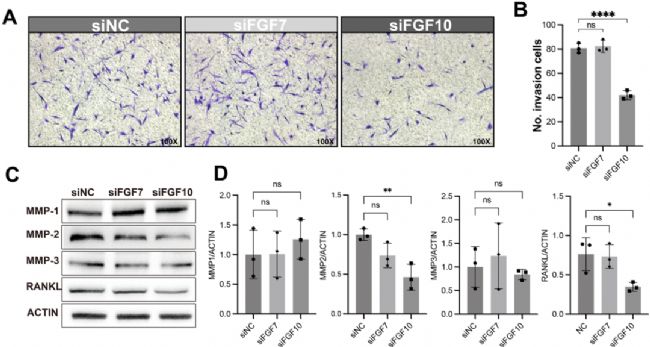
圖6
參考文獻:
X h Meng, Z ch Chen, T Li , et al. Role and Therapeutic Potential for Targeting Fibroblast Growth Factor 10/FGFR1 in Relapsed Rheumatoid Arthritis[J]. Arthritis Rheumatol,2023.