LNP的穩定性對mRNA-LNP疫苗的質量、儲存條件和保質期長短的影響
《mRNA-LNP疫苗的結構與穩定性》文獻解讀系列六
LNP穩定性
除了mRNA 的完整性外,LNP 的穩定性對于 mRNA-LNP 疫苗的質量也至關重要。目前的mRNA疫苗沒有披露關于LNP 穩定性測試的數據,但 Onpattro (patisaran) 的siRNA-LNP 制劑保存在2~8°C 之間時具有三年的有效期,同時該產品不能冷凍保存。
Onpattro 的LNP 系統的組成是:可電離的陽離子脂質DLin-MC3-DMA、DSPC、膽固醇、PEG2000-C-DMG(見表 1)(摩爾比 50:10:38.5:1.5),它們在組成上類似于 Comirnaty 和 mRNA-1273的LNP。在一項siRNA-LNPs 的研究中用類脂質306O 13代替DLin-MC3-DMA,樣品水溶液在 2°C 、pH 7 的環境下下能穩定儲存156 天,其粒徑和siRNA包封率沒有明顯變化。Suzuki 等人的補充研究表明 siRNA-LNP 能在 4°C 環境下穩定儲存1.5。總之,這些數據都表明是mRNA 的不穩定,而不是 LNP 的不穩定,導致了當前mRNA-LNP疫苗的儲存條件嚴苛和保質期短。
Fan等人總結了脂質體和 LNP的穩定性及其質量屬性。LNP 可以承受化學和物理不穩定性,化學不穩定性包括 LNP 中易水解和氧化的脂質的降解。脂質氧化可能發生在不飽和脂肪酸部分(Comirnaty 和 mRNA-1273 不存在該問題)和膽固醇,氧化可能是PEG2000 -DMG中PEG基團存在雜質導致的結果。除此之外,氧化性雜質也可能導致包封的mRNA 氧化。脂質例如 DSPC 和可電離的陽離子脂質中的羧酸酯鍵容易受溫度和pH依賴性的水解的影響(圖 6)。
LNP 穩定性的另一個關鍵因素是物理穩定性,主要有三種類型的物理不穩定性:包封的藥物的聚集、融合和泄漏。 LNP 在儲存和流通過程中容易發生 LNP 的聚集,所以為了增加穩定性,LNP 中通常添加PEG化脂質,LNP微粒表面的PEG 分子可防止LNP 聚集。
另一種類型的物理不穩定性主要由于mRNA 的泄漏,這主要影響包封產品的穩定性。值得注意的是,包封率通常 > 90%,并且尚未報道過在儲存期間出現mRNA泄露(用RiboGreen監測)的情況。未包封的mRNA(“裸露的mRNA”)幾乎不會被細胞攝取;而且它會迅速被降解,因此無法用于翻譯。
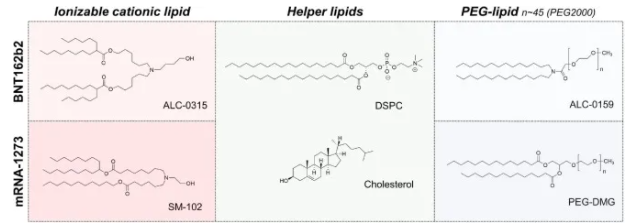
圖6 用于 mRNA-LNP疫苗BNT162b2 (Comirnaty) 和 mRNA-1273的脂質。
由于注射 mRNA-LNP疫苗時的超敏反應可能與PEG化脂質有關,因此,已經研究了防止聚集體形成的替代脂質。使用多聚肌氨酸修飾脂質能使脂質遞送系統更加穩定,在防止LNP聚集的同時能夠減少超敏反應。但是目前仍然需要更多的實驗來確定這種 PEG化脂質替代品是否能真正的提高 mRNA 的穩定性(例如不含過氧化物,注:目前使用的PEG脂質由于工藝原因,會有一定的過氧化物雜質,這會引起LNP中其他含有不飽和鍵的脂質和mRNA的氧化降解)。
分析 LNP 穩定性
Fan 等人在前面提到的文章中對監測 LNP 穩定性的分析方法進行了專業評估。我們推薦感興趣的讀者可以查看相關文獻。
mRNA-LNP中哪個成分更不穩定?
迄今為止,已有幾項研究考察了在儲存期間穩定 mRNA 和穩定 LNP 的方法。然而,兩者之中哪一個才是mRNA-LNP穩定性的瓶頸?當mRNA-LNP 制劑未冷凍時,是mRNA 降解?還是 LNP 降解導致穩定性問題?還是 mRNA 與 LNP 的組合?
與mRNA-LNP 系統相比,包封化學修飾且高度穩定的siRNA 分子(例如 Onpattro)的LNP系統具有更長的有效期。這表明當前的穩定性瓶頸不是 LNP,而是 mRNA。
迄今為止,公開資料還沒有披露關于 mRNA-LNP 制劑中 mRNA 和 LNP 完整性的研究報告。在研究存儲效果的少數研究中,例如 Zhang等人的研究,并沒有考察長期儲存的穩定性。因此,我們將首先研究裸露的mRNA的長期穩定性,但需要注意的是,這可能與包封在 LNP中的 mRNA 的穩定性有所不同(見下文)。
在Pascolo等人的綜述中,裸露的mRNA的水溶液在無RNase的情況下只能在4°C下儲存幾天。這似乎符合目前對 mRNA 不穩定性的看法。目前關于裸露的mRNA長期穩定性的研究表明,mRNA 需要冷凍或干燥才能保持更長時間的穩定。
Roesler等人2009年的研究表明,編碼熒光素酶的mRNA 在無RNA酶存在的條件下,分別以液體或凍干形式在室溫下儲存,表達效率分別在第8天和第16天開始出現降低,凍干輔料和凍干工藝方面未經優化(見圖 7)。同時本研究無法得出關于2-8℃溫度下長期儲存穩定性的結論,因為穩定性研究只考察了32 天。
Wayment-Steele等人經過基于理論降解速率計算,預測 長度為4000 nt的mRNA在 pH 7.4 和5 °C 的條件下,存儲的半衰期為 941 天。他們注意到較長的mRNA序列,例如SAM,更容易發生水解。由于這是jin基于水解降解動力學的理論計算結果,可能會低估 了mRNA的實際降解速率,例如,當存在痕量RNase時,必須對 mRNA 的穩定性進行更多研究才能知道mRNA實際存儲的穩定性情況。
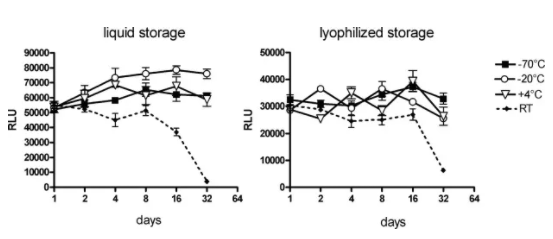
圖7 通過轉染BHK-21細胞中熒光素酶表達效率分析mRNA在水中的穩定性
這些研究表明,在水溶液中 mRNA 可能不如 LNP 穩定。然而,應該重申的是,這兩種成分的穩定性考察結果可能與LNP包封mRNA 的情況不同。如前幾節所述,mRNA 與可電離的陽離子脂質、膽固醇和水一起位于 LNP 核內部(參見圖 4)。這意味著 mRNA 處于水性環境中,因此容易發生水解,其水解的機制可能與溶液中 mRNA水解 的機制相似。然而,另一方面,LNP 內的 mRNA 可能通過疏水、氫鍵和/或靜電相互作用被可電離的脂質包裹。在這種情況下,mRNA 可能比溶解在水溶液中的裸露的mRNA更穩定。在沒有進一步研究的情況下,只能得出結論,mRNA 的不穩定性導致了儲存條件苛刻。
儲存條件不同的原因
當前 mRNA 疫苗的另一個有趣方面是,不同廠家疫苗報告的儲存溫度和相應的“有效期”差異很大:從 -80°C 到 2-8°C,從幾天到幾個月。是否因為mRNA 疫苗處的不同導致這種儲存條件的差異?又或者,儲存條件的差異是否與熱穩定性測試結果相關或更可靠的方法有關?這些信息很重要,因為深入了解對穩定性產生積極影響的因素可能是未來設計熱穩定mRNA 疫苗的關鍵突破點。
Acuitas Therapeutics的首席執行官Tom Madden 曾經在采訪中表示,Moderna 和 Pfizer/BioNTech mRNA 疫苗可能具有相同的穩定性。后者是否有可能使用更保守的方法來確保穩定性?盡管如此,目前必須在 -60 至 -80 °C 之間儲存的Pfizer/BioNTech mRNA-LNP 疫苗很可能也在更高的溫度和冷藏條件下進行了穩定性考察,正如CureVac 科學家所做的那樣。
此外,穩定性測試中的分析技術在靈敏度上可能不同,驗收標準也可能不同。疫苗穩定性研究報告的發布可能對這些疑問作出回答,對此進行比較研究會是很有趣的工作。
文獻來源:
1. Abdelwahed, W., Degobert, G., Stainmesse, S., Fessi, H., 2006. Freeze-drying of
nanoparticles: Formulation, process and storage considerations. Adv. Drug Deliv.
Rev. 58 (15), 1688–1713. https://doi.org/10.1016/j.addr.2006.09.017.
2. Yanez Arteta, M., Kjellman, T., Bartesaghi, S., Wallin, S., Wu, X., Kvist, A.J.,
Dabkowska, A., Sz´ekely, N., Radulescu, A., Bergenholtz, J., Lindfors, L., 2018.
Successful reprogramming of cellular protein production through mRNA delivered
by functionalized lipid nanoparticles. Proc. Natl. Acad. Sci. U. S. A. 115 (15),
E3351–E3360. https://doi.org/10.1073/pnas.1720542115.
3. Ayat, N.R., Sun, Z., Sun, D.a., Yin, M., Hall, R.C., Vaidya, A.M., Liu, X., Schilb, A.L.,
Scheidt, J.H., Lu, Z.-R., 2019. Formulation of biocompatible targeted ECO/siRNA
nanoparticles with long-term stability for clinical translation of RNAi. Nucleic Acid
Ther. 29 (4), 195–207. https://doi.org/10.1089/nat.2019.0784.
4. Baden, L.R., El Sahly, H.M., Essink, B., Kotloff, K., Frey, S., Novak, R., Diemert, D.,
Spector, S.A., Rouphael, N., Creech, C.B., McGettigan, J., Khetan, S., Segall, N.,
Solis, J., Brosz, A., Fierro, C., Schwartz, H., Neuzil, K., Corey, L., Gilbert, P.,
Janes, H., Follmann, D., Marovich, M., Mascola, J., Polakowski, L., Ledgerwood, J.,
Graham, B.S., Bennett, H., Pajon, R., Knightly, C., Leav, B., Deng, W., Zhou, H.,
Han, S., Ivarsson, M., Miller, J., Zaks, T., 2021. Efficacy and safety of the mRNA-
1273 SARS-CoV-2 vaccine. N. Engl. J. Med. 384 (5), 403–416. https://doi.org/
10.1056/NEJMoa2035389.
5. Ball, R.L., Bajaj, P., Whitehead, K.A., 2016. Achieving long-term stability of lipid
nanoparticles: examining the effect of pH, temperature, and lyophilization. Int. J.
Nanomed. 12, 305–315. https://doi.org/10.2147/IJN.S123062.
6. Bloom, K., van den Berg, F., Arbuthnot, P., 2020. Self-amplifying RNA vaccines for
infectious diseases. Gene Ther. 1–13 https://doi.org/10.1038/s41434-020-00204-y.
Brader, M.L., Williams, S.J., Banks, J.M., Hui, W.H., Zhou, Z.H., Jin, L., 2021.
7. Encapsulation state of messenger RNA inside lipid nanoparticles. Biophys. J. https://
doi.org/10.1016/j.bpj.2021.03.012.
8. Brisco, M.J., Morley, A.A., 2012. Quantification of RNA integrity and its use for
measurement of transcript number. e144–e144 Nucleic Acids Res. 40. https://doi.
org/10.1093/nar/gks588.
9.Burke, P.A., Gindy, M.E., Mathre, D.J., Kumar, V., Prud’homme, R.K., 2013. Preparation
of Lipid Nanoparticles. US 2013/0037977.
10. Buschmann, M.D., Carrasco, M.J., Alishetty, S., Paige, M., Alameh, M.G., Weissman, D.,
2021. Nanomaterial delivery systems for mRNA vaccines. Vaccines 9 (1), 65. https://
doi.org/10.3390/vaccines9010065.